ホーム » 理科 » 化学 » 「濃度」の計算が苦手な方へ! 元研究員がわかりやすく解説 問題1 質量パーセント濃度15%の水酸化ナトリウム(NaOH)溶液の密度は10g /cm3 です。 この水溶液のモル濃度を求めましょう。 ただし、原子量 H=10 O=16 Na=23 とします使用目的 2mol/L が7%出会っているのか計算した。 ご意見・ご感想 molから質量パーセント濃度を出せるようにしてほしい。 アンケートにご協力頂き有り難うございました。 送信を完了しました。 塩酸の濃度変換 のアンケート記入欄 性別質量パーセント濃度 = 溶質 (g) 溶液 (g) ×100より、 60 160 ×100=375 2 (1)答 10g 240g

理科の パーセント濃度 の計算問題 教えて欲しいです 出来なくて Clear
質量パーセント濃度 計算機
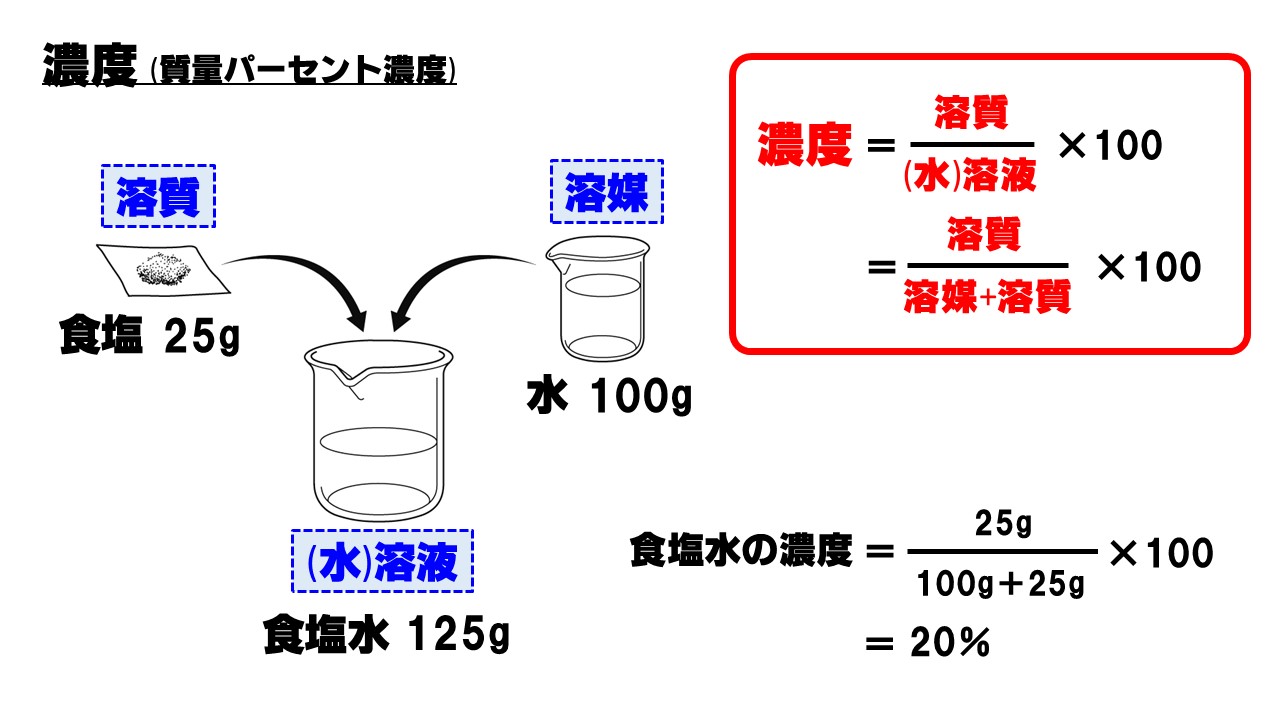
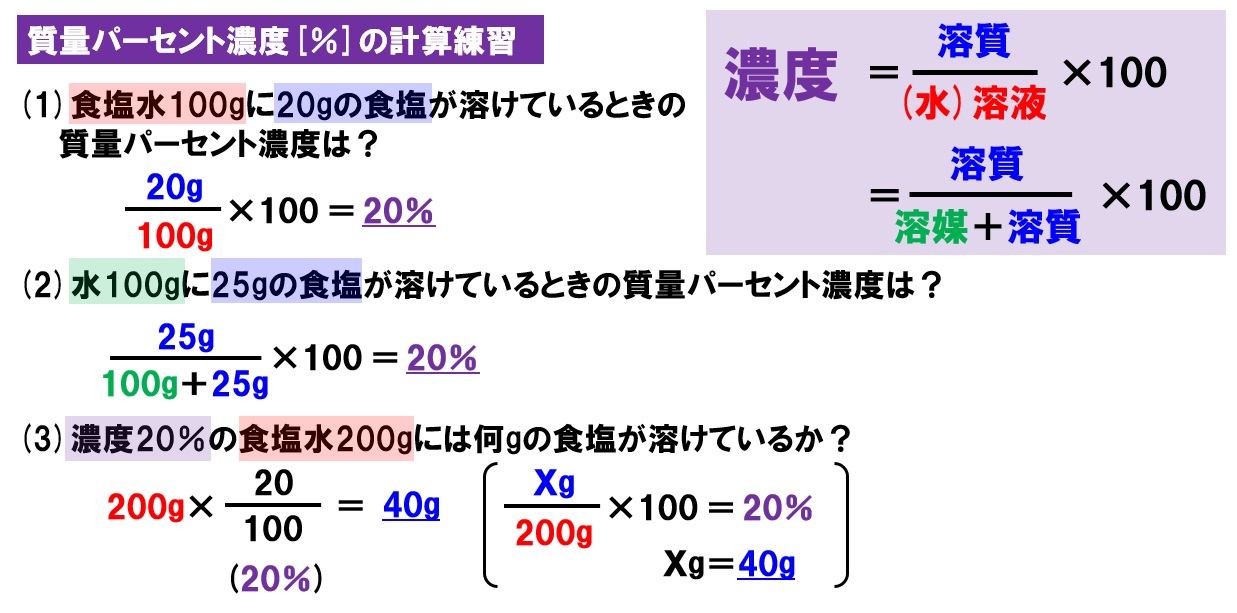
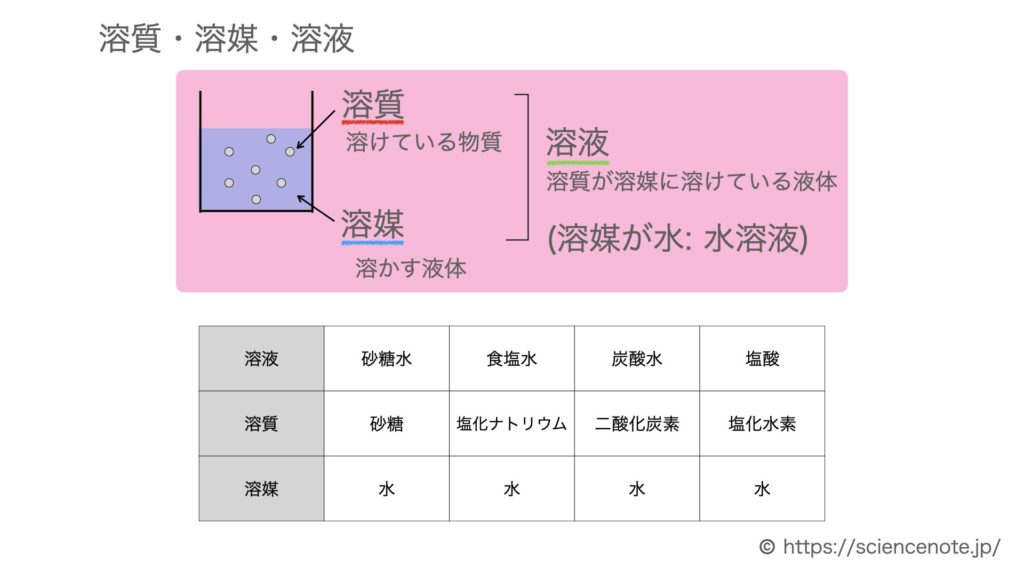
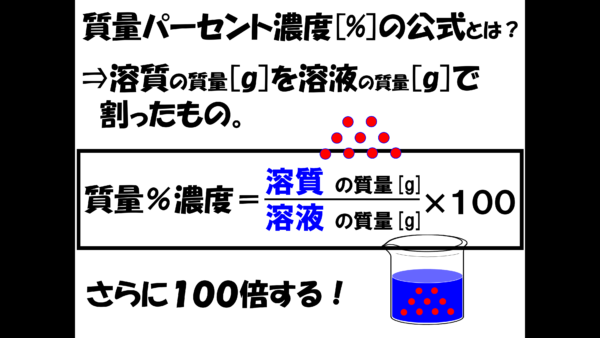
質量パーセント濃度 計算機- 質量パーセント濃度 質量パーセント濃度 とは、その名の通り質量を使って求めた濃度です。 単位は%を使います。 溶液の質量に対して溶質が何g溶けているかを百分率で表したもの です。 次の計算式で求めることができます。溶質の質量を求める 水溶液の濃度の応用問題では、いつも真っ先に 「溶質は何gとけているだろう?」 「水溶液全体の質量は何gだろう?」 の2つを考えることができれば大丈夫です。



中1理科 濃度 質量パーセント濃度 のポイント Examee
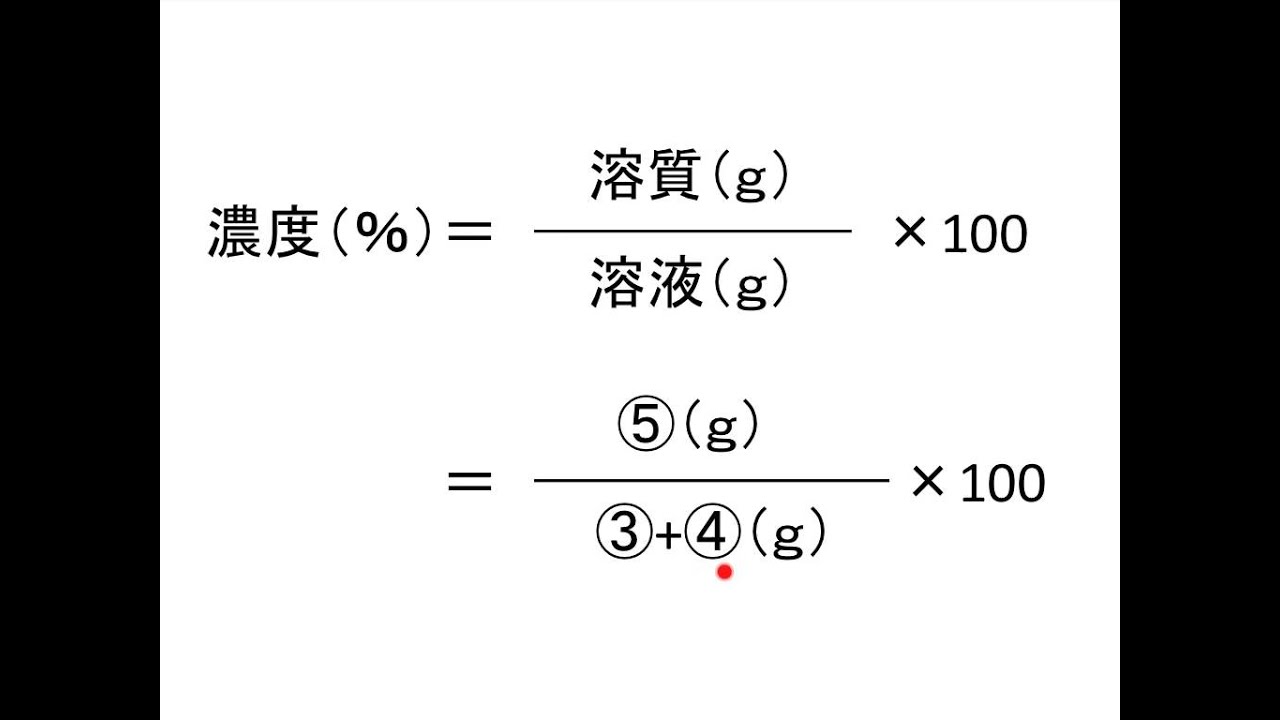
では、実際に計算してみましょう。 溶液の質量は250gで、溶質の質量は50gです。 このことから、質量パーセント濃度は、次のようになります。 (50/250)×100=% よって、答えは、 「%」 となり 質量パーセント濃度を求めるには、公式にあてはめれば一瞬。 質量パーセント濃度は 15% でした。 食塩水が100gあれば、その中に15gの食塩が溶けているくらいの濃さ、ってことです。 ちなみに、とても塩辛い海水でさえ、食塩で考えた質量パーセント濃度は 3~4% です。 質量パーセント濃度の計算 質量パーセント濃度の計算を行う前に、濃度の求め方を復習しましょう。 質量パーセント濃度 = 溶質 / 溶液 ×100 質量パーセント濃度 = 溶質 /(溶媒 + 溶質) ×100 要するに、水溶液全体の質量に対し、溶けている溶質が何%なのかを求めているだけです。
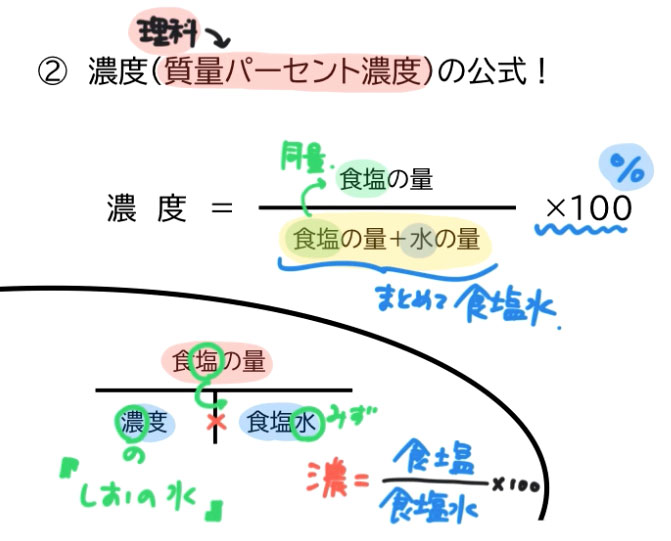
濃度を示す指標として 質量パーセント濃度 があります。これは、溶液100g中に溶質がどれだけ溶けているかを示すものです。 式で表すと、 質量パーセント濃度=溶質÷溶液×100 となります!後ろに100を掛けているのは、出てきた値を百分率で表したいからです。 1.質量パーセント濃度とは、どのような濃度か? 2.モル濃度とは、どのような濃度か? 3.質量パーセント濃度が分かっている溶液のモル濃度を求める手順はどうだったか? お疲れさまでした。 次回からは5章。いよいよ化学反応について考えていきます。濃度換算ツール 質量パーセント濃度、モル濃度、規定度の換算ツールです。 換算種類と物質を選択し、比重と数量の情報を記入した上で換算するボタンを押してください。 このページのトップへ
方程式を使う解き方 求めたい溶媒 (水)の質量を x として解きましょう。 溶質が48g なので、 溶液は (x48)g です。 あとは、 「溶液 × 濃度 = 溶質」 の式で解きます。濃度溶解度 チェックテスト 質量パーセント濃度を求めよ。(割り切れない場合小数第2位で四捨五入) 500gの水溶液の中に溶質が35g溶けている場合。 7% 300gの水溶液の中に溶質がg溶けている場合。 67% 水60gに溶質gを溶かした場合。 25% 水180gに溶質gを溶かした場合。質量パーセント濃度 % 溶液の質量 g 質量パーセント濃度 % = 溶質の質量 g × 100 溶媒の質量 g 溶質の質量 g 溶液の質量 g =



中1理科 水溶液と濃度 水溶液の性質と濃度計算 Pikuu
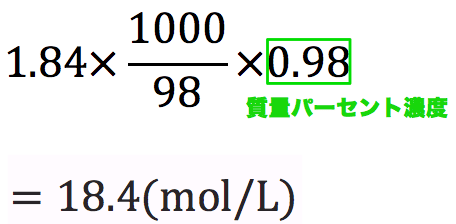



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ
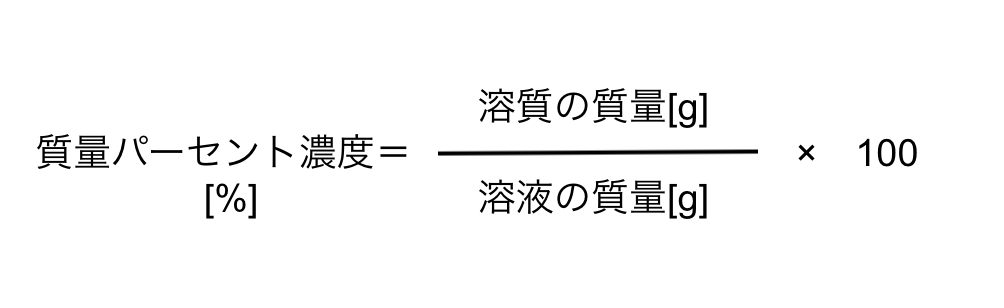
中学校ྕ科 計算༞題習プリントᶱ ഓ 組 ⽒ 1.ෝは、4種࿖のศ質のಁをෝしたものである。後の各༞いにಢえなさい。 ศ質 エタノール アルミニウム 鉄 ೂ ಁ(g/cm3) 07 7 787 6 (1)エタノール100cm3 の質࿂は何g か。 07×100 ( 7g ) 質量パーセントの計算を行うときは、質量パーセントの合計が100%になることを確認することをお勧めします(数学エラーの検出に役立ちます)。 2736 1430 1 5714 = 質量パーセント濃度とは 次は"質量パーセント濃度"にうつりましょう。 単位:g/g→% $$\frac{溶質の質量(g)}{溶液の質量(g)}\times 100=\%$$ これも非常に単純で、溶液の質量(g)を分母、溶質の質量(g)を分子に持って来た上で「割合」を求めます。




見にくくてすいません 化学の質量パーセント濃度計算で Clear




1分でわかる質量パーセント濃度の公式や求め方 基本を登録者数95万人人気講師がわかりやすく解説 ページ 4 4 Study Z ドラゴン桜と学ぶwebマガジン
水溶液は「質量パーセント濃度の求め方」、 状態変化は「水の状態変化」を押さえておけばいいんじゃないかな! 帰国子女(男子) より 18年2月16日 442 AM ポイント 溶液の質量 = 溶質の質量 溶媒の質量 となります。 溶かしたものと溶けたものの合計した重さのことです。 これを式を使って表してみます。 重 要 濃度(%)=溶質の質量(g)÷ 溶液の質量(g)×100 濃 度 ( % ) 溶 質 の 質 量 ( ) 溶🙃 濃度には、 ・質量パーセント濃度 ・モル濃度 ・質量モル濃度 の3種類がありましたね。 26 「化学の中でも電気分解が特に嫌い」 「電気分解は覚えることが多すぎる」 「せっかく覚えても忘れてしまう」 あなたはこのように感じたことはありませんか?




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




中1理科 数学 食塩水の問題を動画でマスター 公式の覚え方と濃度の計算 マナブレイン
そして質量パーセント濃度の求め方というのは 「質量パーセント濃度(%) 溶質の質量(g) 溶液の質量(g) 溶質の質量(g) 溶質の質量(g)+溶媒の質量(g)」 の式で求めますなので溶け残りは計算しません。 わからない場合はまた聞いてください濃度計算 質量パーセント濃度を求めよ。(割り切れない場合は小数第1位を四捨五入して整数で答えよ) 0gの水溶液の中に、溶質が30gが溶けている場合。 水460gに溶質40gを溶かした水溶液。 150gの水溶液のうち、100gが溶媒の場合。 次の問いに答えよ。②『質量パーセント濃度』 drill_02docx (25KB) drill_02_answerdocx (48KB) ③『溶解度』 drill_03docx (107KB) drill_03_answerdocx (118KB) ④『圧力』 drill_04docx (38KB) drill_04_answerdocx (57KB) ⑤『化学変化と物質の質量』 drill_05docx (51KB) drill_05_answerdocx (67KB)



化学基礎モル濃度の計算問題です 類題3 1 質量パーセント濃度が Yahoo 知恵袋




質量パーセント濃度に関する問題です 0 4がどこから出てきたのかわかりません Clear
ハードル2:パーセントは単位ではない 6:左は濃度005、右は濃度0048でよい(質量で比較した濃度) → 濃度にパーセントをつける必要はない → しかし、より分かりやすくするためにパーセントという接尾語をつける 濃度のはなし~中学生向け 質量パーセント濃度について~ 21年2月1日 学習内容解説ブログサービスリニューアル・受験情報サイト開設のお知らせ 学習内容解説ブログをご利用下さりありがとうございます。 開設以来、多くの皆様にご利用いただいてW/v% は,質量体積パーセント濃度,若しくは質量容積パーセント濃度といい,分子が溶質 溶質の質量の質量g で分母が溶液の体積mL の場合であり,w/v% =×100 で表す。溶液の体積



1




モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ
ボリュームパーセントは、 溶質(溶かしている物質)のリットル $\div$ 全体のリットル で計算できます。 例えば、$8\\mathrm{mL}$ のエタノールと $92\\mathrm{mL}$ の水を混ぜて、$100\\mathrm{mL}$ の混合液を作ったとき、エタノールの濃度(vol%)は、 $8\div 100=008$体積パーセント濃度の例 また、「重量」は実際に質量です。 Also see スポーツドリンクの有効性 科学 パーセント構成から簡単な数式を計算する水酸化ナトリウムの質量パーセント濃度をモル濃度に変換します。 0 % 以上 522 % 以下の誤差 (標準偏差)は ± mol/L です。 本ライブラリは会員の方が作成した作品です。 内容について当サイトは一切関知しません。




質量 パーセント 濃度 計算 風人



中1理科 数学 食塩水の問題を動画でマスター 公式の覚え方と濃度の計算 マナブレイン




高校理論化学 溶液の濃度と調製 質量パーセント濃度 密度とモル濃度の単位換算 受験の月




中学理科 計算問題 質量パーセント濃度の計算 Youtube




高校化学基礎 密度とモル濃度 映像授業のtry It トライイット




腎臓 計算に必要な基礎知識 濃縮率の求め方 せいぶつ農国




濃度について 質量パーセント W W と質量体積パーセント W v 生涯学人 まなびと 楽しいサイエンス 暮らしはサイエンス 子供たち サイエンスを感じて




4番教えてください 計算の仕方がわからないです Clear



Q Tbn And9gcsb1uq7n3ghpdmmm6bnifzarmojtjzs00fu7ldneg50py0pkw Usqp Cau




高校化学 質量モル濃度 映像授業のtry It トライイット
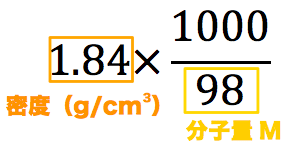



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ




モル計算 濃度計算などの問題 解説 レベルa2 ともよし塾 受験と科学の解説授業




中1理科 濃度 質量パーセント濃度 のポイント Examee



基礎化学3 溶液
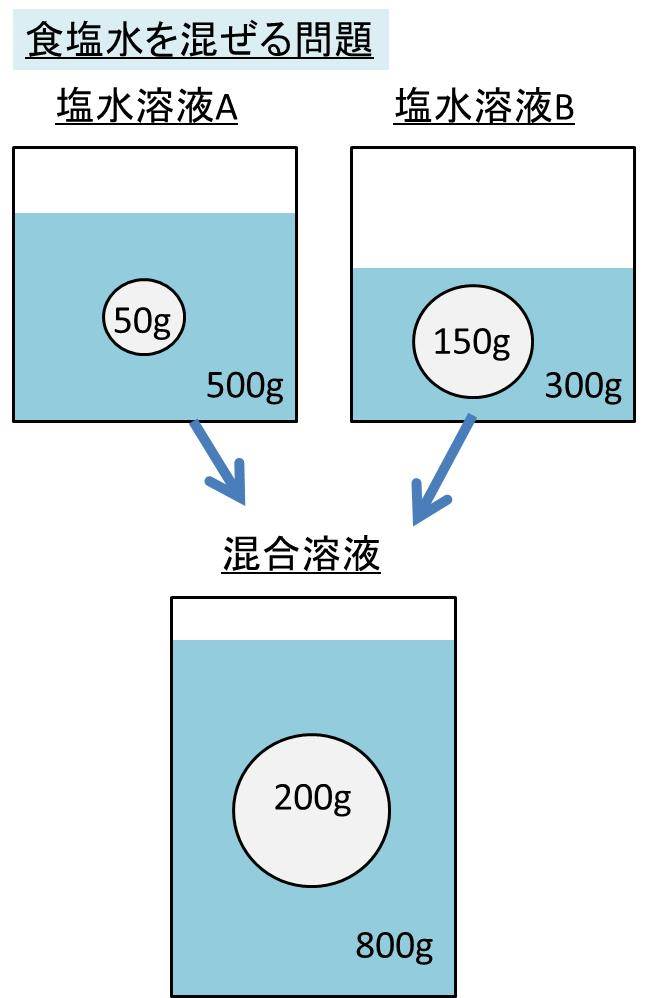



Spi 異なる濃度の食塩水を混ぜる問題の計算方法 濃度算



Thinkstock Images




濃度計算機 For Android Apk Download



水溶液と質量パーセント濃度の計算問題 Hiromaru Note




質量パーセント濃度の計算問題集 基本編 Menon Network




Learn De Leon 家庭教師 ランデレオン 理科 計算 公式 質量パーセント濃度 割合 Facebook




中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu



H30 1 4 4 質量パーセント濃度 On Vimeo




モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ




モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ




E Descubre Como Resolverlo En Qanda
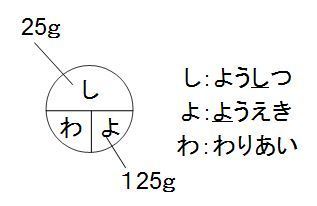



しわよ で覚える質量パーセント濃度 中学テスト 入試対策ノート



質量パーセント濃度中1です 理科の質量パーセント濃度が解けませ Yahoo 知恵袋



中1 理科 飽和水溶液 濃度 溶解度の重要ポイント 札幌市 西区 琴似 発寒 塾 学習塾 個別指導塾 マナビバ



中1理解の 質量パーセント濃度 公式ですが く も わみ Yahoo 知恵袋




Learn De Leon 家庭教師 ランデレオン 理科 計算 公式 質量パーセント濃度 割合 Facebook




高校化学基礎 質量パーセント濃度とは 映像授業のtry It トライイット




質量パーセント濃度




質量パーセント濃度 モル濃度の変換方法を攻略しよう 化学 アイドル好きのホームページ



濃度の求め方 絵で覚えよう Youtube



Q Tbn And9gcrmko2escnl1cjnurstd0t5dmb X3sdynktao5o9vpdvv4txntd Usqp Cau




濃度 の計算が苦手な方へ 元研究員がわかりやすく解説 Study Z ドラゴン桜と学ぶwebマガジン




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ




溶液の濃度 無料で使える中学学習プリント




5問2 質量パーセント濃度 高校化学計算問題 Youtube




化学基礎 モル濃度と質量パーセント濃度の計算問題 Tekibo




中1理科 水溶液 濃度の計算が10分で理解できる たけのこ塾 勉強が苦手な中学生のやる気をのばす
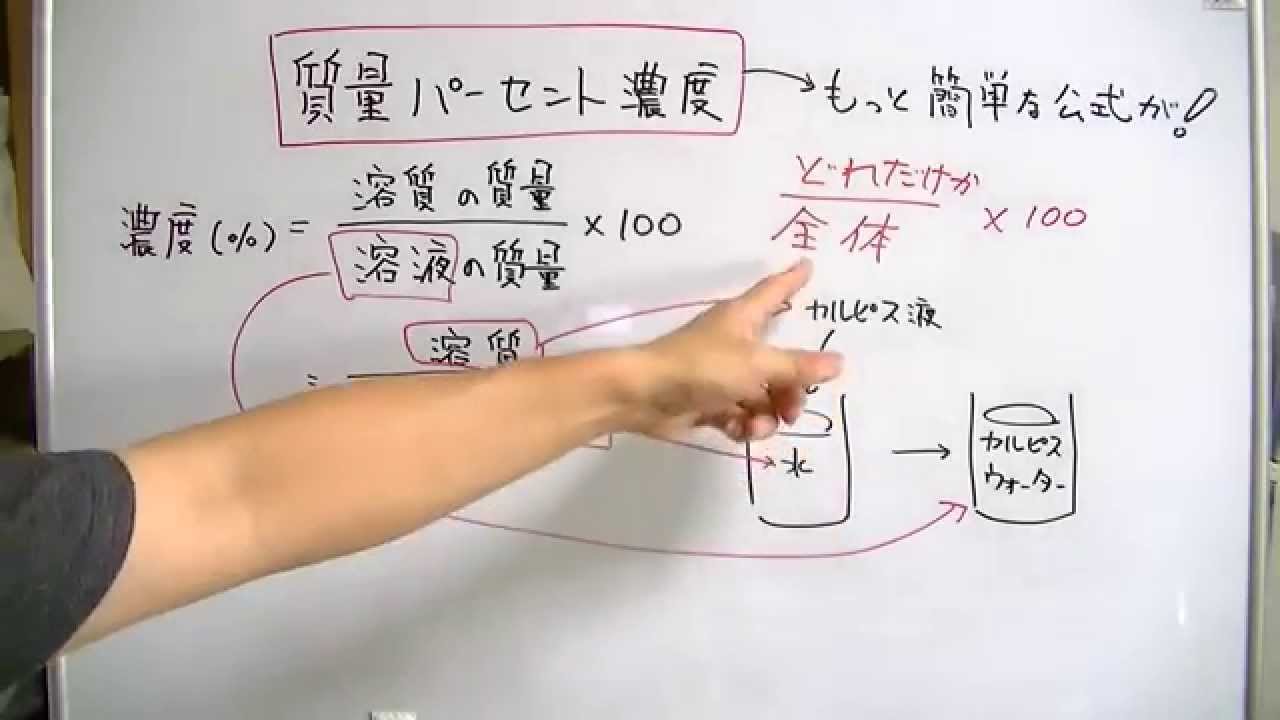



質量パーセント濃度 簡単な公式で覚えよう おときち副塾長 電脳空間学習塾かもん Youtube




Akiya Su En Twitter 理科 質量パーセント濃度 溶質 溶媒 溶液と公式を覚えること 計算は難しくないが 割り算の筆算で小数点の位置がわからない人は先生に聞こう 中学理科 質量パーセント濃度




質量パーセント濃度の求め方 問題を使ってかんたんに解説するぞ 中学数学 理科の学習まとめサイト



溶質を求める




化学勉強法 センター試験09 Mol濃度から質量パーセント濃度へ 大村の化学勉強法




4 6 溶液の濃度 おのれー Note




50g 50g 0 24 Descubre Como Resolverlo En Qanda




高校化学基礎 硫酸とモル濃度 映像授業のtry It トライイット



質量パーセント濃度の計算問題が出てきた 21年02月08日の人物のボケ 07 ボケて Bokete




高校化学基礎 濃度の計算 練習編 映像授業のtry It トライイット



Www City Matsumoto Nagano Jp Kodomo Gimukyoiku Shochu Junior High School J Sugano Sonota Shidou Rika Tyuu1 Minomawari Bussitu Files Situryou Per Noudo Pdf



10倍に薄めてない食酢中の質量パーセント濃度はいくらか 食酢 Yahoo 知恵袋
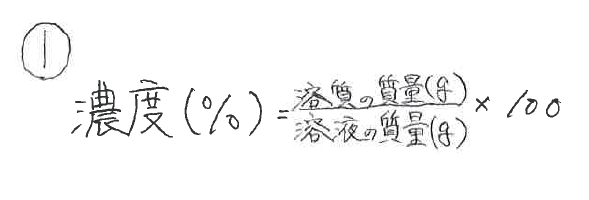



濃度のはなし 中学生向け 質量パーセント濃度について 学習内容解説ブログ



H30 1 4 4 質量パーセント濃度 On Vimeo




1 150 G G Descubre Como Resolverlo En Qanda



金魚の薬浴のための0 5 食塩水の作り方 質量パーセント濃度 金魚道楽




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




Learn De Leon 家庭教師 ランデレオン 理科 計算 公式 質量パーセント濃度 割合 Facebook



1




1 15 600g5 Descubre Como Resolverlo En Qanda




理科の パーセント濃度 の計算問題 教えて欲しいです 出来なくて Clear




問2から分かりません 答え見ても計算が合いません 解説お願いします Clear




Wt 重量パーセント Mass 質量パーセント とは 計算方法は 演習問題
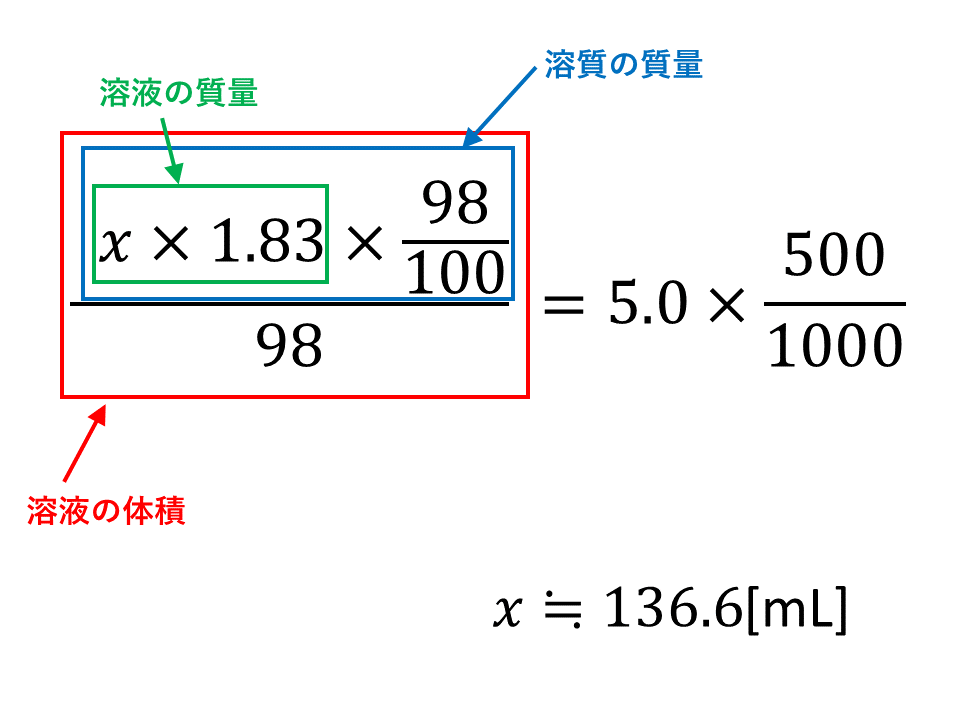



モル濃度と密度 質量パーセント濃度の考え方 Vicolla Magazine




化学 濃度の計算 オンライン無料塾 ターンナップ




モノマナビ研究所



水溶液と質量パーセント濃度の計算問題 Hiromaru Note




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




理科 中1 27 質量パーセント濃度 Youtube
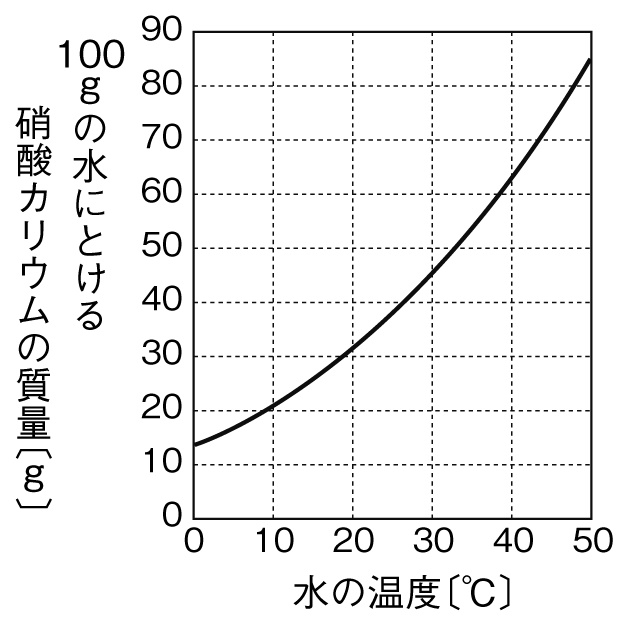



定期テスト対策問題 質量パーセント濃度の計算演習問題 Examee




中1 理科 中1 32 質量パーセント濃度 Youtube
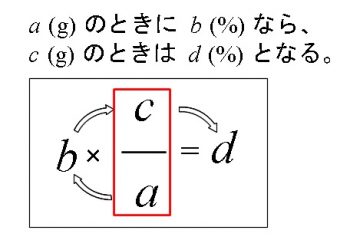



溶液の質量パーセント濃度の求め方と比重を利用した計算問題




中1 理科 質量パーセント濃度の計算 P塾



モル濃度 質量パーセント濃度 質量モル濃度 濃度計算のコツも解説 受験メモ




質量パーセント濃度の計算問題集 応用編 Menon Network




質量パーセント濃度 中学生 理科のノート Clear




4 6 溶液の濃度 おのれー Note
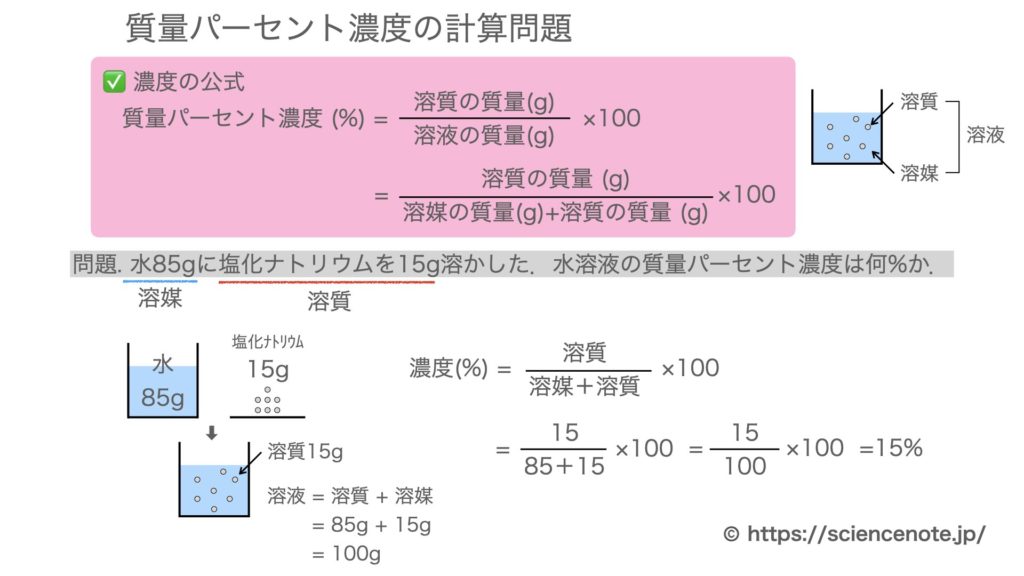



水溶液と質量パーセント濃度の計算問題 Hiromaru Note



受験化学 9 溶解度の計算1 みかみの参考書ブログ
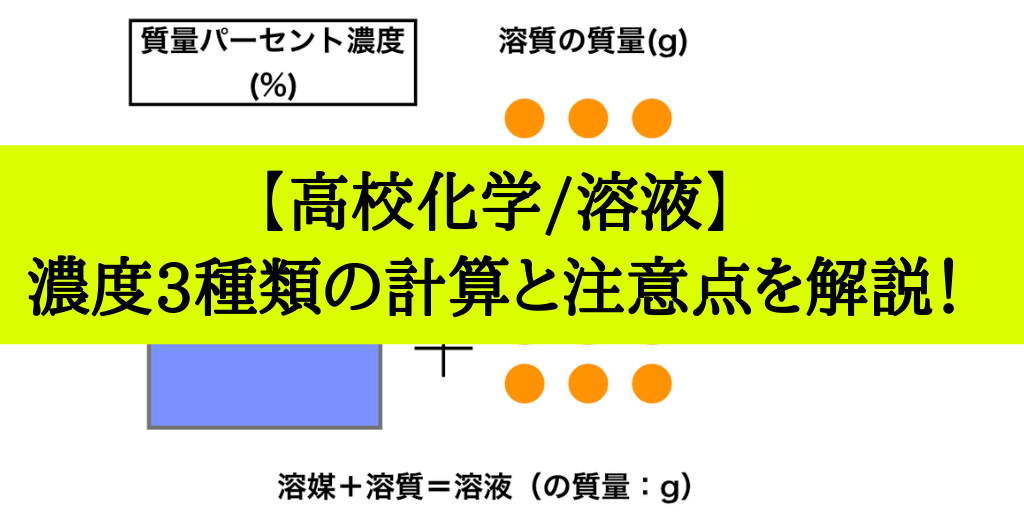



Mol濃度 質量パーセント濃度 質量モル濃度の相互変換の仕方のコツ




密度や質量パーセント濃度の計算の 覚え方を教えてください Clear




中1理科 水溶液 濃度の計算が10分で理解できる たけのこ塾 勉強が苦手な中学生のやる気をのばす
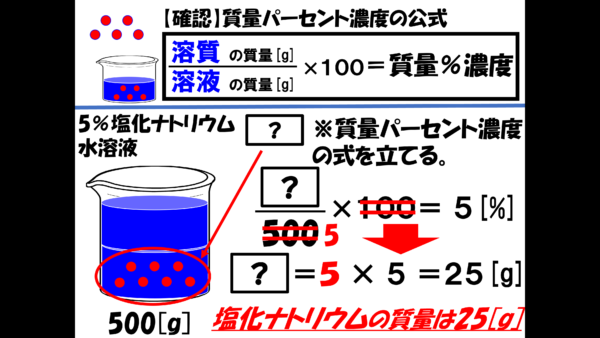



危険物資格取得のための高校化学no 2 濃度計算 F M サイエンスブログ




質量パーセント濃度の求め方とモル濃度の違い



危険物資格取得のための高校化学no 1 濃度計算 F M サイエンスブログ




質量パーセント濃度の問題を計算したのですが どうやっても答えになり 中学校 教えて Goo




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




これで理科マスター 質量パーセント濃度を計算する5つの問題 Qikeru 学びを楽しくわかりやすく



濃度の応用




高校化学基礎 密度とモル濃度 映像授業のtry It トライイット




4 6 溶液の濃度 おのれー Note




6 7 モル濃度と密度から質量パーセント濃度を計算します 1lあったとしたら と仮定すれば あとは簡単です プレテスト化学基礎 第3問 問3 Youtube



0 件のコメント:
コメントを投稿